Молекулярно-генетические исследования неизбежно влияют на внесение изменений в клинические рекомендации. На их основе затем формируются стандарты, меняются подходы к лечению, и это находит отражение в программах государственных гарантий и ОМС. Как ускорить этот процесс? Как сделать так, чтобы новые технологии быстрее вводились в рутинную практику врачей, становились все более доступными для широкого круга пациентов? Эти вопросы обсуждались на прошедшей 26 марта I Всероссийской научно-образовательной конференции «Молекулярно-генетические исследования в практической онкологии: от лабораторных решений до клинической практики». Мероприятие стало площадкой, которая объединила врачей, ученых, организаторов здравоохранения, юристов в их стремлении поднимать и решать проблемы в области молекулярно-генетических исследований.
Тренд на развитие
Постановка качественного диагноза – главная задача в любой сфере медицины. От диагноза зависят и адекватная тактика лечения, и жизнь пациента, и благополучие его близких, и эффективность расходования ресурсов, и юридическая безопасность врача. Молекулярно-генетические исследования (МГИ) вроде бы вошли в рутинную практику, но доступны пока лишь части пациентов.
 Область этой научной деятельности связана со сложностями не только в Российской Федерации. Вопросы, которые находятся на стыке клинической практики, науки и организации медицинской помощи, актуальны для многих стран, отметил генеральный директор ФГБУ «Центр экспертизы и контроля качества медицинской помощи» (ЦЭККМП) Минздрава России, заведующий кафедрой экономики, управления и оценки технологий здравоохранения ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» (РМАНПО) Виталий Владимирович Омельяновский. Поэтому так важен международный опыт клинического применения молекулярно-генетических технологий, который следует учитывать, считает он.
Область этой научной деятельности связана со сложностями не только в Российской Федерации. Вопросы, которые находятся на стыке клинической практики, науки и организации медицинской помощи, актуальны для многих стран, отметил генеральный директор ФГБУ «Центр экспертизы и контроля качества медицинской помощи» (ЦЭККМП) Минздрава России, заведующий кафедрой экономики, управления и оценки технологий здравоохранения ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» (РМАНПО) Виталий Владимирович Омельяновский. Поэтому так важен международный опыт клинического применения молекулярно-генетических технологий, который следует учитывать, считает он.
Эксперт подчеркнул, что особую актуальность обретает образование врачей, поскольку нехватка знаний может ограничивать внедрение новых технологий и снижать их доступность для пациентов. «Мы можем много говорить про финансирование, номенклатуру услуг, стандарты, клинические рекомендации, но если у нас не будет грамотных врачей, работающих на современном уровне лабораторий, мы не сможем обеспечить приход новых инновационных лекарственных препаратов, о которых говорим и которые находятся на разных стадиях разработки», – сказал он.
 В настоящее время в список жизненно важных лекарственных средств входят более 30 препаратов, при назначении которых требуется определение молекулярного профиля опухолей. Более десяти нозологий (самых значимых по численности пациентов) нуждаются в определении молекулярного профиля опухоли. Более того, появляется тенденция к созданию препаратов, которые зарегистрированы для всех типов рака при условии наличия определенного маркера, рассказала профессор кафедры онкологии факультета усовершенствования врачей ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» (РНИМУ им. Н.И. Пирогова) Минздрава России, исполнительный директор Российского общества клинической онкологии (RUSSCO) Вера Витальевна Карасева. По ее словам, эти тренды будут влиять на развитие молекулярно-генетического тестирования и требования к нему.
В настоящее время в список жизненно важных лекарственных средств входят более 30 препаратов, при назначении которых требуется определение молекулярного профиля опухолей. Более десяти нозологий (самых значимых по численности пациентов) нуждаются в определении молекулярного профиля опухоли. Более того, появляется тенденция к созданию препаратов, которые зарегистрированы для всех типов рака при условии наличия определенного маркера, рассказала профессор кафедры онкологии факультета усовершенствования врачей ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» (РНИМУ им. Н.И. Пирогова) Минздрава России, исполнительный директор Российского общества клинической онкологии (RUSSCO) Вера Витальевна Карасева. По ее словам, эти тренды будут влиять на развитие молекулярно-генетического тестирования и требования к нему.
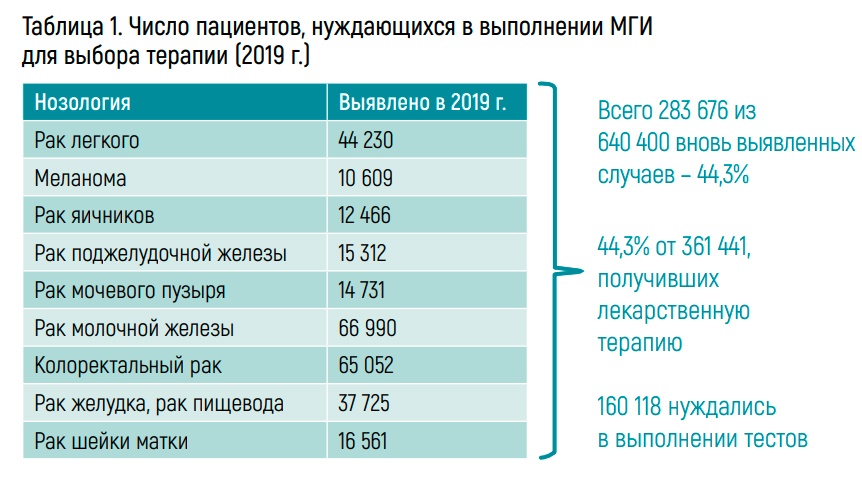
Согласно данным, которые она привела, в 2019 г. 361 441 пациент получил лекарственную терапию, среди них примерно 160 тыс. нуждаются в молекулярно-генетическом тестировании. «Мы должны помнить, что для этих пациентов требуется тестирование не одного, а нескольких маркеров.
Поэтому это тоже влияет на объемы финансирования и развитие подходов к молекулярно-генетическому и иммуногистохимическому тестированию», – сказала она.
Нужен объединяющий документ
Говоря о роли профессиональных сообществ в развитии персонализированной медицины, В.В. Карасева отметила, что благодаря партнерству нескольких профессиональных организаций создано уже более 80 клинических рекомендаций в онкологии, как минимум в десяти из них отмечена потребность в МГИ. Деятельность профессиональных организаций направлена на обновление клинических рекомендаций при появлении новых биомаркеров и препаратов, на обучение лабораторий новым видам тестирования, а также контроль качества тестирования и подготовку практических рекомендаций по МГИ. В числе перспективных направлений молекулярно-биологических исследований были названы внедрение новых методик тестирования – NGS (секвенирование нового поколения), внедрение новых маркеров и тестов в новых биообразцах, жидкостная биопсия.
Если необходимость в обновлении клинических рекомендаций ни у кого не вызывает сомнения, то по вопросу, следует ли создавать отдельные документы по молекулярному тестированию, в профессиональном сообществе пока не удалось достичь единого мнения. Сегодня вопрос ставится следующим образом: дополнять ли уже существующие клинические рекомендации по злокачественным новообразованиям проведением МГИ или разработать один документ, посвященный исключительно МГИ; необходимо ли указывать конкретные методы проведения МГИ в клинических рекомендациях или оставить врачу выбор метода в каждом конкретном клиническом случае?
 По мнению заведующей кафедрой онкологии и паллиативной медицины им. академика А.И. Савицкого ФГБОУ ДПО РМАНПО Минздрава России Ирины Владимировны Поддубной, на сегодняшнем этапе, учитывая особенности законодательства, создавать отдельные клинические рекомендации по молекулярному тестированию не следует: «Я считаю, что все должно носить прикладной характер. Компонент должен быть в каждой нозологии, где он имеет значение. Мне представляется, что подобное решение наиболее адекватно отражает задачи клинических рекомендаций».
По мнению заведующей кафедрой онкологии и паллиативной медицины им. академика А.И. Савицкого ФГБОУ ДПО РМАНПО Минздрава России Ирины Владимировны Поддубной, на сегодняшнем этапе, учитывая особенности законодательства, создавать отдельные клинические рекомендации по молекулярному тестированию не следует: «Я считаю, что все должно носить прикладной характер. Компонент должен быть в каждой нозологии, где он имеет значение. Мне представляется, что подобное решение наиболее адекватно отражает задачи клинических рекомендаций».
В.В. Омельяновский выразил полное согласие с такой позицией. Он напомнил коллегам: «У нас есть клинические рекомендации, есть номенклатура медицинских услуг, в конце концов, есть методические рекомендации, технологические карты медицинских услуг. Клинические рекомендации – это не то место, где надо подробно описывать, как проводить процедуру. Документ, который носит абсолютно прикладной, технический характер, может называться методическими рекомендациями, на которые можно ссылаться в клинических рекомендациях. Но клинические рекомендации – в первую очередь для врачей, а не для генетиков или врачей-лаборантов. Если хочешь, ты переходишь по ссылке, где прописано, как это делать, но это не основная часть клинических рекомендаций». У RUSSCO своя позиция на этот счет.
Некий объединяющий документ, безусловно, нужен, согласилась И.В. Поддубная. Но им может стать утверждаемое Минздравом методическое руководство, считает она: «Это не методическое пособие, а методическое руководство – в нем можно осветить проблему с разных сторон. Я думаю, это будет мультидисциплинарный проект с участием авторского коллектива, и это может быть очень востребованный, нужный, полноценный продукт – методическое руководство».
В.В. Омельяновский обратил внимание участников конференции на те достижения, которые есть в области подготовки клинических рекомендаций в России. Во-первых, удалось устранить дублирование – по одному заболеванию теперь есть одна клиническая рекомендация, что облегчает специалистам работу. Во-вторых, в разработке клинических рекомендаций сейчас участвует не одна ассоциация, а несколько ассоциаций, иногда даже междисциплинарных, что, на взгляд эксперта, очень ценно. «К тому, что создано Минздравом в нормативном поле, можно по-разному относиться, но какие-то промежуточные результаты достигнуты. Мы унифицируем подходы, исключаем дублирование клинических рекомендаций, все больше и больше побуждаем разных специалистов участвовать в рабочих группах по разработке клинических рекомендаций», – перечислил он успехи.
В.В. Омельяновский добавил, что есть и другая сторона, которую в профессиональном сообществе не все еще осознают. «Если я разработчик инновационных подходов и у меня появляется новая технология, я с ней бегаю по рынку, по официальным учреждениям, органам исполнительной власти, не понимая, куда идти. Сейчас унификация этого нормативного поля привела к тому, что появляется системный подход к внедрению инноваций, абсолютно понятный, системный, логичный трек. Я должен включить свою разработку в клинические рекомендации, что должно найти отражение в стандартах помощи. Это произойдет тогда, когда она будет зарегистрирована как медицинское изделие либо как медицинская услуга. Когда это попадает в стандарты, профессиональные сообщества, ассоциации, главные специалисты, НМИЦ должны бороться за то, чтобы инновация стала критерием качества медицинской помощи (если тому есть определенные доказательства) и квалификационным критерием в формировании клинико-статистических групп. Тогда мы понимаем, что кроме всяких коммерческих продвижений появляется абсолютно системный, прозрачный путь погружения инноваций в систему ОМС либо в систему государственного финансирования медицинской помощи».
МГИ в программе госгарантий
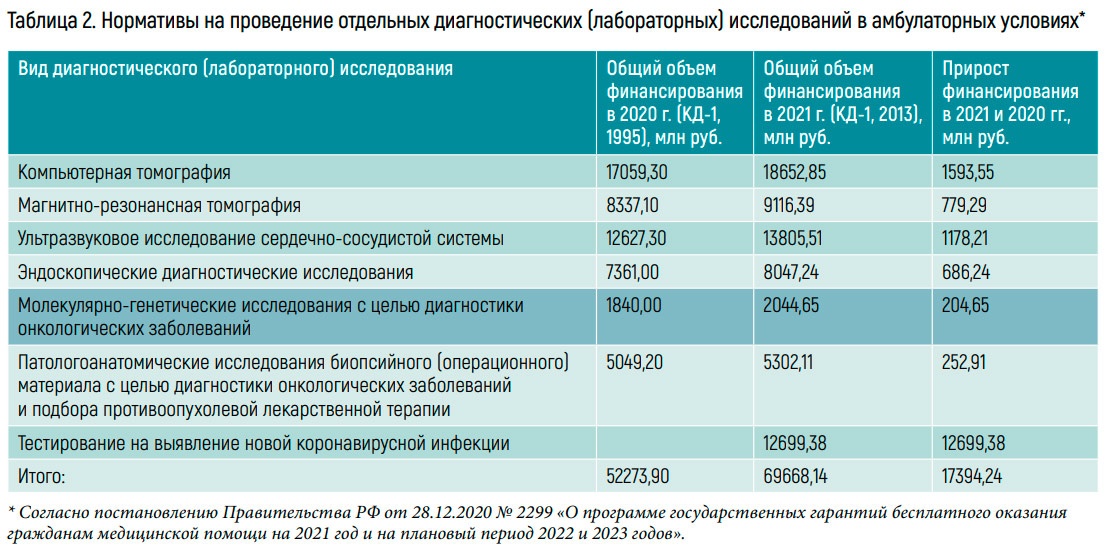
 В 2020 г. произошло важное для отрасли событие – МГИ для диагностики онкологических заболеваний были погружены в программу государственных гарантий, выделено дополнительное финансирование в размере 1,8 млрд рублей, в 2021 г. сумма была увеличена до более 2 млрд рублей. «Деньги на финансирование МГИ в программе госгарантий заложены, имеются, и уже второй год мы работаем в условиях, когда данные исследования являются гарантированными для пациентов», – сказала заместитель генерального директора ФГБУ ЦЭККМП Минздрава России Инна Александровна Железнякова.
В 2020 г. произошло важное для отрасли событие – МГИ для диагностики онкологических заболеваний были погружены в программу государственных гарантий, выделено дополнительное финансирование в размере 1,8 млрд рублей, в 2021 г. сумма была увеличена до более 2 млрд рублей. «Деньги на финансирование МГИ в программе госгарантий заложены, имеются, и уже второй год мы работаем в условиях, когда данные исследования являются гарантированными для пациентов», – сказала заместитель генерального директора ФГБУ ЦЭККМП Минздрава России Инна Александровна Железнякова.
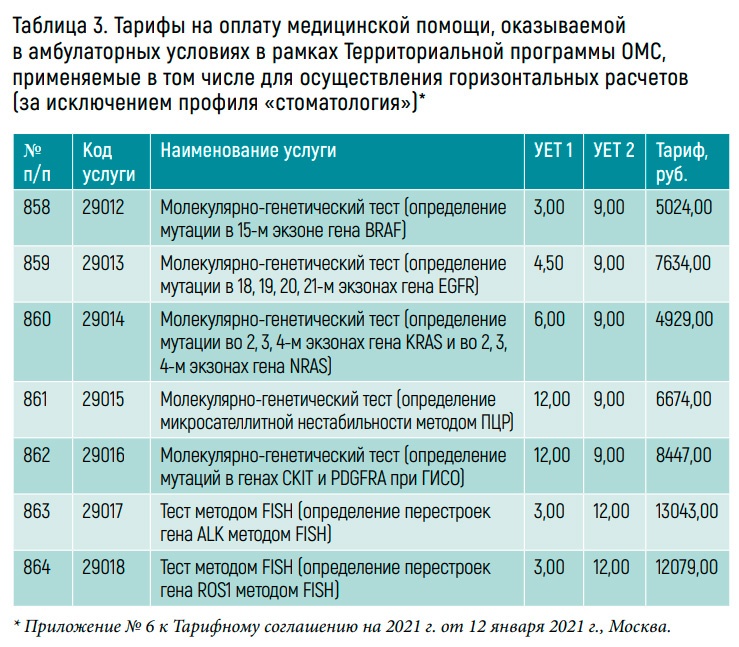
Она отметила, что согласно программе госгарантий тарифы на данные исследования не могут включаться в подушевой норматив финансирования вне зависимости от способа оплаты, то есть при применении любых способов оплаты на МГИ должны устанавливаться отдельные тарифы. В 2021 г. пересмотрены подходы к формированию среднего норматива объема МГИ с целью диагностики онкологических заболеваний, изменен подход к определению единицы объема медицинской помощи: он определен как исследование биопсийного (операционного и диагностического) материала с применением одного теста – для данного вида опухоли в соответствии с клиническими рекомендациями по лечению онкологических заболеваний. Учитывая, что в 2020 г. под средним нормативом понимался комплекс исследований, значения нормативов объемов и стоимости проведения МГИ в 2021 г. соответственно скорректированы. «Существенные изменения связаны с изменением единицы планирования. Мы видим, что стоимость в 2021 г. с 15 000 руб. снизилась до 9 800 руб., но объемный норматив, напротив, увеличился практически пропорционально изменению цены.
И связано это не с понижением стоимости, а с тем, что изменилась единица планирования: если в 2020 г. это был комплекс исследований, то в 2021 г. это один тест. Стоимость меньше – норматив больше», – прокомментировала И.А. Железнякова.
Также в 2021 г. формулировка «гистологические исследования» и единицы учета при формировании норматива объема были приведены в соответствие с правилами проведения патологоанатомических исследований, утвержденными приказом Минздрава России от 24.03.2016 № 179н (формулировка изменена на «патологоанатомические исследования биопсийного (операционного) материала», а единица учета изменена с «объекта биопсийного (операционного) материала» на «случай прижизненного патологоанатомического биопсийного (операционного) материала»). Также с 2021 г. изменился подход к определению норматива исследований: в него была включена возможность применения дополнительных методов окрасок (постановок реакций, определений – гистохимических, иммуногистохимических и иных методов), что привело к соответствующей корректировке значений нормативов объема и финансовых затрат на единицу объема.
В программе госгарантий для субъектов установлено, что те нормативы, которые они будут устанавливать в своих территориальных программах, могут корректироваться в зависимости от заболеваний, методов исследований, которые применяются в регионе, то есть могут изменяться исходя из конкретной ситуации в регионе. «В программе госгарантий и в сопроводительном письме к ней об экономическом обосновании конкретизировано, что является единицей норматива – это исследование биопсийного материала с применением одного теста. Норматив рассчитан как средневзвешенная стоимость одной реакции (теста) для данной опухоли. Важно, что данный норматив включает в том числе расходы на транспортировку диагностического материала к месту исследования и расходы на хранение образца», – уточнила эксперт. Регулируется и порядок назначения всех диагностических исследований, на которые установлены отдельные нормативы, в том числе молекулярно-генетические. Направление на эти исследования осуществляется врачом, оказывающим первичную медико-санитарную помощь, в том числе специализированную (эта позиция появилась в 2021 г.) медицинскую помощь.
И.А. Железнякова отметила, что нормативы в программе госгарантий – это именно нормативы, субъектам переданы полномочия устанавливать тарифы самостоятельно, с учетом применяемых видов исследований.
Она подчеркнула, что установлен и максимально детализирован норматив для медицинской помощи в амбулаторных условиях, в условиях же стационара и дневного стационара МГИ также могут оказываться, но уже за счет средств сверх данного норматива. В сопроводительном письме к программе госгарантий приведен основной перечень МГИ, которые предположительно должны выполняться, а также объемы планирования регионом этого вида медицинской помощи и ее финансового обеспечения.
«К сожалению, в 2021 г. был исключен коэффициент сложности лечения пациента в случае, если МГИ проводилось в круглосуточном стационаре. То, что пациенту было проведено дополнительное исследование как таковое, не является сложностью его курации, это просто дополнительный метод исследования, и применять коэффициент к данной процедуре идеологически было не совсем правильно. Но на сегодняшний день в рамках клинико-статистических групп (КСГ), конечно, больницы могут и должны выполнять МГИ, если у пациента не может быть осуществлен забор материала в иных условиях. Но при этом в рамках тарифа по КСГ какой-то дополнительной оплаты в 2021 г. для этого не предусмотрено», – пояснила эксперт. В условиях дневного стационара выделена отдельная КСГ, включающая взятие биопсии, а также полный комплекс молекулярно-генетических и иммуногистохимических исследований. И все-таки главной проблемой МГИ в регионах, которая вызывает больше всего нареканий, остается их доступность в рамках программы госгарантий на всей территории Российской Федерации, признала И.А. Железнякова. В частности, отсутствуют рекомендации по установлению тарифов на МГИ на федеральном уровне. Нет возможности выполнять все виды таких исследований в рамках программы госгарантий в каждом субъекте. В тарифе на оплату стационарной медицинской помощи не учтены затраты на МГИ, вследствие чего закупить такие исследования у сторонней организации медорганизация, которая не выполняет их самостоятельно, может только за счет собственных средств. Есть сложности с их закупкой и у медорганизаций, работающих в амбулаторных условиях, поскольку тариф предусматривает только сами исследования, соответственно между тарифом и закупочной ценой всегда будет дифференциация, которая может быть расценена как незаконное обогащение.
Возникают и сложности с межтерриториальными расчетами ввиду того, что доставка материала включается в тариф, но тариф устанавливается для медицинской организации, выполняющей иссле дование, которой сложно организовать доставку из всех субъектов РФ. При этом ТФОМС по месту выполнения исследования не всегда готов устанавливать тарифы, учитывающие доставку из разных регионов, а для медицинской организации, направившей материал, нет возможности установить тариф только на доставку.
Возможный вариант решения в данной ситуации – медицинская организация по месту исполнения анализа сама организует доставку, но при этом территориальный фонд по месту выполнения исследования должен устанавливать тарифы, включающие доставку. Причем, как настаивают медицинские организации, тарифы должны быть максимально дифференцированы в зависимости от региона, потому что стоимость доставки из разных регионов – например, с Дальнего Востока или из Центрального федерального округа – совершенно разная. «Пока сложно с тем, чтобы территориальный фонд по месту нахождения медорганизации дифференцировал тарифы для своей медорганизации с учетом доставки из других субъектов», – признала представительница ЦЭККМП. И отметила в то же время, что ряд субъектов и медорганизаций уже имеют такой положительный опыт.
Вследствие проблем с межтерриториальными расчетами возникают сложности с оплатой услуг, оказываемых референс-центрами, а также с погружением телемедицинских услуг в подушевой норматив финансового обеспечения. И.А. Железнякова представила возможные подходы, которые, на ее взгляд, могли бы исправить ситуацию и повысить доступность МГИ. Для этого, предлагает она, надо:
- разработать на федеральном уровне рекомендации по установлению тарифов на МГИ;
- предусмотреть в тарифах на оплату стационарной медпомощи возмещение затрат на проведение МГИ;
- включить в нормативы программы госгарантий и соответственно в тариф на оплату медпомощи в амбулаторных условиях расходы на забор биологического материала для проведения МГИ.
Эксперт также рекомендовала дать возможность устанавливать тарифы только на транспортировку биологического материала, а для всех медорганизаций, оказывающих помощь по профилю «онкология», установить необходимость заключения договоров с референс-центрами, в которых бы предусматривалась оплата услуг в рамках межучрежденческих расчетов. Кроме того, И.А. Железнякова высказалась за централизацию оплаты МГИ в референс-центрах аналогично оплате специализированной медицинской помощи в федеральных медорганизациях.
Рассчитать потребности
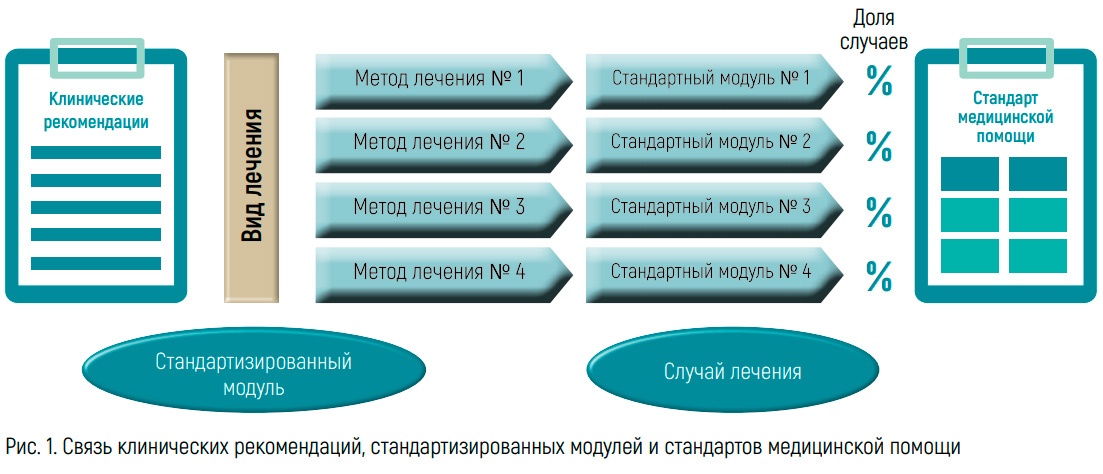
 Сегодня процесс взаимодействия и взаимосвязи клинических рекомендаций и стандартов медицинской помощи определен на законодательном уровне – в Федеральном законе № 323 «Об основах охраны здоровья граждан в Российской Федерации», а также в ряде нормативных правовых актов. В 2018 г. в онкологии впервые был реализован переход к оплате медицинской помощи дифференцированно по схемам химио терапии. Апробировано это было с помощью методологии формирования так называемых стандартизированных модулей. Как пояснила доцент кафедры экономики, управления и оценки технологий здравоохранения ФГБОУ ДПО РМАНПО Минздрава России, начальник отдела методического обеспечения стандартизации ФГБУ ЦЭККМП Минздрава России Юлия Анатольевна Ледовских, стандартизированный модуль – это инструмент, который позволяет оцифровать клинические рекомендации, отразить методы лечения, которые в них описаны, структурированно, в виде табличных форм, с указанием медицинских услуг, лекарственных препаратов, то есть формализовать объем медицинской помощи. Таблицы позволяют структурировать информацию, определить цифровые значения для тех или иных элементов, вероятность их использования в популяции пациентов. Это дает материал, с которым могут работать экономисты, поскольку становится возможным просчитать и оценить объемы потребностей, в том числе в части лекарственных препаратов. То же касается МГИ: если они есть в клинических рекомендациях, появляется возможность оцифровать, просчитать и определить вероятность их использования в популяции пациентов.
Сегодня процесс взаимодействия и взаимосвязи клинических рекомендаций и стандартов медицинской помощи определен на законодательном уровне – в Федеральном законе № 323 «Об основах охраны здоровья граждан в Российской Федерации», а также в ряде нормативных правовых актов. В 2018 г. в онкологии впервые был реализован переход к оплате медицинской помощи дифференцированно по схемам химио терапии. Апробировано это было с помощью методологии формирования так называемых стандартизированных модулей. Как пояснила доцент кафедры экономики, управления и оценки технологий здравоохранения ФГБОУ ДПО РМАНПО Минздрава России, начальник отдела методического обеспечения стандартизации ФГБУ ЦЭККМП Минздрава России Юлия Анатольевна Ледовских, стандартизированный модуль – это инструмент, который позволяет оцифровать клинические рекомендации, отразить методы лечения, которые в них описаны, структурированно, в виде табличных форм, с указанием медицинских услуг, лекарственных препаратов, то есть формализовать объем медицинской помощи. Таблицы позволяют структурировать информацию, определить цифровые значения для тех или иных элементов, вероятность их использования в популяции пациентов. Это дает материал, с которым могут работать экономисты, поскольку становится возможным просчитать и оценить объемы потребностей, в том числе в части лекарственных препаратов. То же касается МГИ: если они есть в клинических рекомендациях, появляется возможность оцифровать, просчитать и определить вероятность их использования в популяции пациентов.
Финальным этапом этого процесса является формирование стандарта – ответственность за это лежит на главных внештатных специалистах, за методологическое же обеспечение процесса отвечает Центр экспертизы и контроля качества медицинской помощи Минздрава.
Его задача – соблюдение методологии, преемственности подходов от профиля к профилю, в том числе информации, которая отражена в клинических рекомендациях, с той информацией, которая будет отражена в стандартах медицинской помощи. И это при том, что в каждом профиле клинические ситуации и подходы к лечению пациентов разнятся, и даже в рамках одного профиля каждое заболевание имеет свои особенности течения, ведения, маршрутизации пациентов, пояснила Ю.А. Ледовских сложность задачи. Поэтапно процесс выглядит следующим образом.
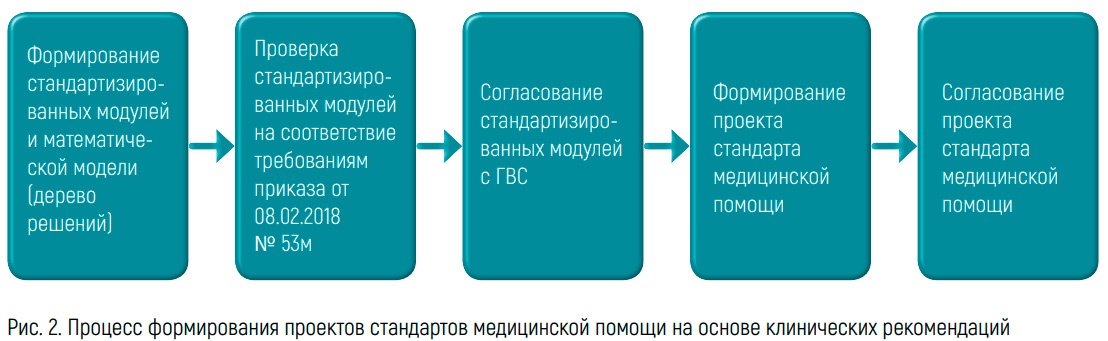
На первом этапе главные внештатные специалисты или их представители совместно со специалистами Центра экспертизы формируют стандартизированные модули по утвержденной методологии. Далее эти модули подвергаются экспертизе, после чего весь материал направляется главным внештатным специалистам и их экспертам. После очередного пересмотра при необходимости специалисты возвращают материал на первый этап, вновь вносят какие-либо изменения в стандартизированный модуль и математическую модель. После чего модули согласовываются, а дальше формируется стандарт медицинской помощи, причем этот процесс происходит по сути на основе просто математических действий.
Как отметила Ю.А. Ледовских, проект стандарта медицинской помощи бывает не совсем понятен клиницистам, поскольку они не видят в нем отражения процесса движения пациента по клинической рекомендации. «Но здесь важно понять, что для онкологических и онкогематологических заболеваний, которые по большей части бывают длительными, этапы течения заболевания выделяются в клинических рекомендациях. И получается, что объем медицинской помощи для пациентов разнится в зависимости от года ее оказания: в год постановки диагноза лечение может быть более интенсивным и соответственно будут применены одни методы, в последующие годы – другие методы», – пояснила она. Вероятность обращения пациента за медицинской помощью, появление тех или иных рецидивов, прогрессирование заболевания – все это отражается экспертами в виде математической модели, которая потом позволяет правильно просчитать и описать объем медицинской помощи на усредненный пациенто-год вне зависимости от условий ее оказания.
«То есть стандарт не регламентирует, что должно быть сделано на сегодняшний день в стационаре, дневном стационаре, амбулаторно, потому что есть другие нормативные правовые акты, в том числе определяющие подходы к оплате медицинской помощи, которые могут разниться от субъекта к субъекту в плане каналов финансирования.
Субъект может сам правильно сбалансировать свою территориальную программу, опираясь на те данные, которые представлены в стандарте медицинской помощи, где описан объем помощи, необходимый в соответствии с клиническими рекомендациями», – указала Ю.А. Ледовских. Она заметила, что есть несколько «но» в этой области. Первое – то, что в стандарты медицинской помощи не включаются лекарственные препараты off-label. «Важно понимать, что стандарт медицинской помощи не равен тарифу на оплату, поскольку тарифы формируются иначе. Вместе с тем данные, которые формируются в процессе разработки стандартов, могут быть использованы для расчета тарифов, для формирования предложений по совершенствованию способов опла ты, но не следует воспринимать это буквально», – рекомендовала она. Еще одно большое «но» касается МГИ. В соответствии с приказом Минздрава России от 28.02.2019 № 103н, утвердившим порядок и сроки разработки клинических рекомендаций, эти документы формируются тезисно, четко и понятно, для того чтобы быстро и правильно донести информацию до практикующего врача, дать ему понимание, какую тактику выбирать в той или иной клинической ситуации. При этом разработчикам клинических рекомендаций нередко приходится сталкиваться с таким моментом, как отсутствие в номенклатуре медицинских услуг той или иной услуги, того или иного медицинского изделия.
Она уточнила, что сегодня процедура подачи предложения для включения медицинских услуг в номенклатуру определена. На сайте Центра экспертизы и контроля качества медицинской помощи есть форма, которую могут заполнить специалисты, в том числе принимающие участие в разработке стандартов и клинических рекомендаций, и подать предложение о включении тех или иных МГИ в номенклатуру. МГИ могут быть не включены только по одной причине – если нет зарегистрированных расходных материалов, которые необходимы для проведения данной медицинской услуги, оговорила эксперт. Вообще работа над стандартами поднимает много вопросов, призналась Ю.А. Ледовских. Работа по профилю «онкология» впервые началась в 2017 г., когда по поручению министра попытались оцифровать клинические рекомендации, для того чтобы рассчитать финансовую потребность в оказании медицинской помощи. Тогда Центр экспертизы первый раз поднял вопрос о действующей номенклатуре и внесении в нее необходимых исследований, которые описаны в клинических рекомендациях и которые нужны для назначений, в том числе лекарственных препаратов.
Это стало толчком к переутверждению номенклатуры, в том числе в части МГИ, с возможностью просчитать затраты на использование лекарственных препаратов в рамках нацпроекта.
Приказ Минздрава России от 13.10.2017 № 804н «Об утверждении номенклатуры медицинских услуг» полностью систематизирует подходы в части МГИ. По словам Ю.А. Ледовских, ЦЭККМП ведет работу по совершенствованию номенклатуры медицинских услуг с целью приведения их классификации к единообразию. Она оговорила при этом: «Но нужно понимать, что если в 2020–2021 гг. произошла регистрация каких-либо медицинских изделий, то в любом случае будет присутствовать какой-то временной лаг. Потому что номенклатура утверждается приказом, эта процедура имеет свои временные требования, поэтому не может происходить в режиме реального времени, отставания всегда будут».
Отсутствуют правила и системный подход
 Одна из основных проблем в области МГИ – это отсутствие правил их выполнения. В действующих нормативных актах они упоминаются фрагментарно, эпизодически, полноценного системного подхода у регулятора пока нет, заявила вице-президент фонда «Вместе против рака», учредитель юридической компании «Факультет медицинского права», адвокат Полина Георгиевна Габай. Она представила рекомендации по внедрению патолого-морфологических и молекулярно-генетических исследований в практическую онкологию, включая нормативно-правовое регулирование. Так, в действующих нормативных актах, например в Правилах проведения патологоанатомических исследований, утвержденных приказом Минздрава России от 24.03.2016 № 179н, имеются лишь эпизодические упоминания МГИ. Однако имеющиеся нормы не дают понимания многих важных аспектов, например, о методиках, оборудовании, штатной укомплектованности, не содержат требований к лабораториям для проведения МГИ, порядку направления биологического материала на исследование, форме такого направления, срокам проведения исследования.
Одна из основных проблем в области МГИ – это отсутствие правил их выполнения. В действующих нормативных актах они упоминаются фрагментарно, эпизодически, полноценного системного подхода у регулятора пока нет, заявила вице-президент фонда «Вместе против рака», учредитель юридической компании «Факультет медицинского права», адвокат Полина Георгиевна Габай. Она представила рекомендации по внедрению патолого-морфологических и молекулярно-генетических исследований в практическую онкологию, включая нормативно-правовое регулирование. Так, в действующих нормативных актах, например в Правилах проведения патологоанатомических исследований, утвержденных приказом Минздрава России от 24.03.2016 № 179н, имеются лишь эпизодические упоминания МГИ. Однако имеющиеся нормы не дают понимания многих важных аспектов, например, о методиках, оборудовании, штатной укомплектованности, не содержат требований к лабораториям для проведения МГИ, порядку направления биологического материала на исследование, форме такого направления, срокам проведения исследования.
Как сообщила П.Г. Габай, 4 марта 2021 г. был опубликован проект приказа Минздрава России об утверждении Правил проведения лабораторных исследований. Однако и данный документ не учитывает специфику проведения МГИ, не устанавливает каких-либо особенностей их организации и проведения. Необходимо определить правила проведения МГИ в качестве отдельного вида исследований, проводимых при оказании медицинской помощи.
Нет единых подходов и правил и в деле лицензирования и штатной укомплектованности специалистов, которые работают в лабораториях с МГИ. В постановлении Правительства РФ от 16 апреля 2012 г. № 291 о лицензировании медицинской деятельности среди врачебных и доврачебных услуг медицинская генетика и гистология не значатся вовсе. Не отражены они и в иных нормативных правовых актах. Очевидно, что услуги, закрепленные в номенклатуре, не покрывают всего разнообразия МГИ, заключила юрист и высказалась за их включение в номенклатуру медицинских услуг, клинические рекомендации и стандарты медицинской помощи. «Какие специалисты кроются за данными услугами в настоящее время, абсолютно неизвестно. Если мы говорим о специалистах, то здесь важно понимать, что входит в объем их трудовых функций», – указала она.
Что касается профессиональных стандартов, то некоторые из них уже утверждены: врач-генетик, врач-патологоанатом, специалист в области клинической лабораторной диагностики, специалист в области лабораторной диагностики со средним медицинским образованием. Однако в каждом из этих нормативных актов есть свои нестыковки и недоработки, заметила П.Г. Габай.
Кроме того, нуждается в коррекции номенклатура медицинских услуг, утвержденная приказом Минздрава России от 13.10.2017 № 804н. Услуги, закрепленные в номенклатуре, не покрывают всего разнообразия МГИ. Например, для исследования мутаций в генах BRCA1 и BRCA2 в крови (или в биопсийном материале) не определен метод МГИ. По словам П.Г. Габай, «услуга в номенклатуре висит в каком-то неполноценном виде, хотя данное исследование выполняется довольно широко и даже набор реагентов, используемый в этой сфере, прошел регистрацию».
Она напомнила, что еще в 2018 г. Минздрав заверил: если что-то не вошло в номенклатуру, это совершенно не критично, потому что услуги могут оказываться за пределами номенклатуры. «Либеральный подход министерства хорош, но он упирается в проблемные зоны, потому что номенклатура медицинских услуг является основой для формулирования стандартов медпомощи. Далее, если мы идем по цепочке, то стандарты медпомощи ложатся в основу базовой программы ОМС и даже в порядок подготовки клинических рекомендаций. Понятно, что нужно номенклатуру дорабатывать», – высказалась юрист.
Говоря о клинических рекомендациях по группе заболеваний «опухоли невыявленной первичной локализации», П.Г. Габай обратила внимание на то, что уровень их убедительности разнится, налицо определенная недоработанность. Нужно собирать рабочую группу, которая бы занялась дополнением данных документов. Далее в полном объеме молекулярные исследования могут лечь в стандарты медицинской помощи.
На взгляд регулятора
 Государственная регистрация медицинских изделий в России – это долгий и нелегкий процесс, который может занимать до полутора лет. Но, как сообщил заместитель руководителя Росздравнадзора Дмитрий Юрьевич Павлюков, здесь ожидаются подвижки. Хотя ключевая проблема в регистрации тестов для МГИ заключается, на его взгляд, в нежелании самого производителя проводить данную процедуру. Например, в ведомстве часто сталкиваются с тем, что производители секвенаторов не заинтересованы в их выводе на российский рынок, потому что придется раскрывать технические характеристики, чтобы показать, что тест-система работает эффективно и безопасно. Сложность представляет и сбор большого объема клинического материала – у большинства компаний нет такой возможности. Росздравнадзору известно, что многие медицинские организации применяют незарегистрированные изделия для медицинской практики.
Государственная регистрация медицинских изделий в России – это долгий и нелегкий процесс, который может занимать до полутора лет. Но, как сообщил заместитель руководителя Росздравнадзора Дмитрий Юрьевич Павлюков, здесь ожидаются подвижки. Хотя ключевая проблема в регистрации тестов для МГИ заключается, на его взгляд, в нежелании самого производителя проводить данную процедуру. Например, в ведомстве часто сталкиваются с тем, что производители секвенаторов не заинтересованы в их выводе на российский рынок, потому что придется раскрывать технические характеристики, чтобы показать, что тест-система работает эффективно и безопасно. Сложность представляет и сбор большого объема клинического материала – у большинства компаний нет такой возможности. Росздравнадзору известно, что многие медицинские организации применяют незарегистрированные изделия для медицинской практики.
«Мы прекрасно понимаем, что много подобного оборудования ввозилось и ввозится для научных исследований. Законодательство Евразийского экономического союза сегодня это позволяет. Мало того, корреспондирующие с ЕЭС нормы выгружаем в национальное законодательство, потому что не видим здесь никаких проблем. Такое оборудование должно и может ввозиться без разрешения для использования в научных целях. Но ставить по ним диагнозы, определять лечение – это совершенно другая степень ответственности и степень доказательства качества эффективности и безопасности медицинских изделий», – сказал Дмитрий Павлюков.
Для того чтобы урегулировать ситуацию в данной области, в Росздравнадзоре обратились к международной практике. Выход был подсказан прозрачной системой, практикуемой в США: разработанная в медицинской организации тест-система в формате этой медицинской организации может применяться без государственной регистрации. Точно такие же подходы примени ли в России, когда прорабатывали поправки по установлению особенностей обращения незарегистрированных медицинских изделий. Чиновник уточнил, что речь идет о готовящихся изменениях в Федеральном законе № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации». В нем появится новая статья, которая установит особенности обращения незарегистрированных медицинских изделий для диагностики in vitro, разработанных и применяемых в медицинских организациях. Это позволит медицинской организации, которая выстроит у себя стандартные операционные процедуры, обеспечивающие повторяемость качественного результата таких исследований, подав заявку регулятору и пройдя проверку с его стороны, применять незарегистрированный тест в медицинских целях. В ближайшие месяцы правительство внесет такие изменения в соответствующем порядке в Государственную Думу, сообщил чиновник. Д.Ю. Павлюков оговорил, что такая процедура будет доступна не по всем видам медицинских изделий, это коснется только изделий для диагностики in vitro и только тех, которые на сегодняшний день не имеют зарегистрированных на рынке аналогов.
Кроме того, она будет доступна не всем юридическим лицам, а только тем, кто действительно занимается наукой и имеет базис для развития и поддержания соответствующих технологий. Также будет установлен ряд критериев для того, чтобы инструмент не превратился в исключительно коммерческий. Такой подход себя оправдает, тем более что он успешно применяется за рубежом.
Делается это в первую очередь для того, чтобы обеспечить нуждающихся пациентов медицинскими изделиями, которые невозможно зарегистрировать в установленном порядке, подчеркнул представитель Росздравнадзора.
Ситуация с финансированием МГИ на сегодняшний день намного лучше, чем это было несколько лет назад – их выполняется и оплачивается все больше. Но проблемные зоны здесь остаются, и всех волнует, что будет дальше и насколько государство готово обсуждать и регулировать эти вопросы. В частности, речь идет о том, что в разных регионах тарифы считаются по-разному, в некоторых они крайне низки, даже ниже базовой ставки, потому что регионам дана свобода в этой сфере. Из-за этого лаборатории отказываются проводить исследования, особенно сложные, новые.
 У Фонда ОМС свой взгляд на ситуацию с финансированием МГИ, показало выступление начальника Управления модернизации системы ОМС Федерального фонда обязательного медицинского страхования Ольги Владимировны Царевой. Она указала на то, что, несмотря на непростую эпидемическую ситуацию, в 2020 г. на противоопухолевую терапию было направлено свыше 210 млрд рублей. Что значительно больше по сравнению с 2019 г., когда начался федеральный проект «Борьба с онкологическими заболеваниями» и на химиотерапию субъектам в рамках системы ОМС было направлено около 117 млрд рублей. «По нашим скромным оценкам, текущий год никак не станет провальным с точки зрения объема финансового обеспечения именно противоопухолевой терапии», – заключила она. На проведение МГИ запланировано направить в 2021 г. свыше 2 млрд руб.
У Фонда ОМС свой взгляд на ситуацию с финансированием МГИ, показало выступление начальника Управления модернизации системы ОМС Федерального фонда обязательного медицинского страхования Ольги Владимировны Царевой. Она указала на то, что, несмотря на непростую эпидемическую ситуацию, в 2020 г. на противоопухолевую терапию было направлено свыше 210 млрд рублей. Что значительно больше по сравнению с 2019 г., когда начался федеральный проект «Борьба с онкологическими заболеваниями» и на химиотерапию субъектам в рамках системы ОМС было направлено около 117 млрд рублей. «По нашим скромным оценкам, текущий год никак не станет провальным с точки зрения объема финансового обеспечения именно противоопухолевой терапии», – заключила она. На проведение МГИ запланировано направить в 2021 г. свыше 2 млрд руб.
«Поэтому сказать, что данный вид исследования недоступен для субъектов либо недостаточно финансируется со стороны федерального фонда в рамках территориальных программ, было бы неправильно», – считает представительница ФФОМС. Она при этом заметила, что остаются отдельные методологические вопросы, которые будут обсуждать на этапе подготовки новой программы госгарантий на следующий год, и отдельные замечания экспертов, возможно, могут быть учтены.
П.Г. Габай на это возразила, что с мест поступает иная информация, и участники рынка ждут, будет ли проблема низких и неравных тарифов урегулирована на федеральном уровне. О.В. Царева ответила, что тезис о недостаточности тарифа ей кажется сомнительным. Во-первых, потому, что у всех лабораторий разные возможности по оборудованию, кадрам и квалификации. Во-вторых, разница в установленных на Сахалине и в Москве тарифах экономически обусловлена, и сравнивать их напрямую методологически неправильно.
Она напомнила, что структура тарифа установлена в соответствии с базовым Федеральным законом № 326-ФЗ «Об обязательном медицинском страховании», а методику расчета тарифа определяет приказ Минздрава России № 108н «Об утверждении Правил обязательного медицинского страхования». Вместе с тем представительница ФФОМС заверила, что в фонде обратят внимание на тарификацию отдельных МГИ и, возможно, в следующем году предусмотрят некие рекомендации по поводу стоимости исследований для субъектов.
П.Г. Габай также подняла вопрос оплаты МГИ в больницах: «Сегодня говорили о том, что тарифа в этой сфере нет, что МГИ входят внутрь случая. В этом плане что-то планируется усовершенствовать?»
О.В. Царева ответила, что решения по данному вопросу пока нет. «Мы подумаем, что в этой части можно сделать и, самое главное, насколько нужно это делать. Чтобы у нас не получалось двойного финансирования одного и того же мероприятия по разным источникам», – обещала она. И призналась, что в ФФОМС пока не очень понимают, насколько востребована данная услуга именно в рамках лечения: «Как правило, это проходит на уровне амбулаторного лечения, где все урегулировано.
Максимум, что проходит в рамках стационарного лечения либо в условиях дневного стационара, это забор материала. Поэтому, думаю, мы еще раз вернемся к этому вопросу, посоветуемся с нашими главными внештатными специалистами – насколько тарифы в рамках хирургического лечения надо уточнять и дополнять, погружать к каким-то усредненным расчетам, в том числе и с проведением МГИ, которые нужны не в каждом случае».